Анатомия лёгких, строение, функции на ONKO.LV
Лёгкие – это мягкий, губчатый, конусообразный парный орган. Лёгкие обеспечивают дыхание — обмен углекислого газа и кислорода. Так как лёгкие являются внутренней средой организма, которая постоянно соприкасается с внешней средой, они имеют хорошо приспособленное и специализированное строение не только для газообмена, но и для защиты – в дыхательных путях задерживаются и выводятся наружу различные вдыхаемые инфекционные возбудители, пыль и дым. Правое лёгкое образуют три доли, а левое — две. Воздух в лёгкие попадает через носовую полость, горло, гортань и трахею. Трахея разделяется на два главных бронха – правый и левый. Главные бронхи разделяются на более мелкие и образуют бронхиальное дерево. Каждая веточка этого дерева отвечает за небольшую ограниченную часть лёгкого – сегмент. Более мелкие веточки бронхов, которые называются бронхиолами, переходят в альвеолы, в которых происходит обмен кислорода и углекислого газа.
Чтобы облегчить движения лёгких, их окружает плевра – оболочка, которая состоит из двух листков – висцеральной и париетальной плевры.
Париетальная плевра присоединяется к стенке грудной клетки. Висцеральная плевра присоединяется к наружней поверхности каждого лёгкого. Между двумя плевральными листками образуется небольшое пространство, которое называется плевральной полостью. В плевральной полости находится небольшое количество водянистой жидкости, которая называется плевральной жидкостью. Она предотвращает трение и держит вместе плевральные поверхности во время вдоха и выдоха.
Строение клеток глубоких дыхательных путей достаточно специализировано и хорошо приспособлено для дыхания. Все дыхательные пути выстланы эпителием, который является специально приспособленными клетками, чтобы выполнять много важных функций:
- защитную;
- секрецию слизи;
- выведение раздражающих веществ;
- начало иммунных реакций.

Вид эпителия отличается в разных частях дыхательных путей. Большую часть слизистой дыхательных путей образует реснитчатый эпителий. Эти клетки – расположены вертикально в один слой с ресничками, направленными в сторону дыхательных путей. Реснички всегда движутся в направлении наружу. Слизистую более мелких дыхательных путей образует эпителий без ресничек.
В эпителии дыхательных путей находятся железы – бокаловидные клетки. Это специализированные клетки, которые производят и выделяют слизь. Слизь, продуцируемая этими клетками необходима, чтобы увлажнять поверхность эпителия и механически защищать слизистую.
Слизь является липкой, поэтому к ней прилипают вдыхаемые микроскопические инородные тела, и потом они выводятся наружу при помощи реснитчатого эпителия.
Поражение легких по типу матового стекла на КТ
Благодаря мультиспиральной компьютерной томографии грудной клетки, или МСКТ, которая считается наиболее информативным методом обследования легких, врачи могут диагностировать инфекционно-воспалительные и онкологические заболевания на ранних стадиях.
«Матовые стекла» характерны для пневмонии, туберкулеза, рака легких и других опасных состояний. Какие именно и по каким признакам их различают? Рассмотрим подробнее в этой статье.
Что такое «матовое стекло»?
«Матовые стекла» — это участки уплотнения легочной ткани, которые хуже пропускают X-Ray лучи. По-другому их называют очагами уплотнения ткани легких. На томограммах такие области напоминают светлые пятна или мутноватый налет. Очаги по типу «матового стекла» свидетельствуют о том, что альвеолы легких заполнены жидкостью (транссудатом, кровью), а не воздухом. Также они могут свидетельствовать о снижении пневматизации легких из-за фиброзных изменений. Альвеолы участвуют в газообмене, снабжают клетки кислородом и выводят углекислый газ, поэтому заполнение их полости жидким веществом или клетками соединительной ткани недопустимо.
Если общая площадь «матовых стекол» увеличивается, это свидетельствует о прогрессирующем инфекционно-воспалительном заболевании. Пациента начинает беспокоить нехватка воздуха, одышка, кашель.
Пациента начинает беспокоить нехватка воздуха, одышка, кашель.
При каких заболеваниях «матовое стекло» проявляется на томограммах?
По данным кафедры лучевой диагностики ММА им. Сеченова, картину «матовости» чаще всего дают пневмонии (вирусные, бактериальные, грибковые), однако инфильтрация легких характерна и для других патологических состояний. Вот только некоторые из них:
- Альвеолярный протеиноз;
- Пневмонит;
- Кровоизлияние;
- Альвеолярный отек;
- Аллергический альвеолит;
- Туберкулез;
- Медикаментозное поражение легких;
- Инфаркт легкого;
- Вирусная инфекция;
- Дерматомиозит;
- Опухоли;
- Ревматоидный артериит;
- Респираторный бронхиолит с ИЗЛ;
- Синдром Съегрена;
- Синдром Гудпасчера;
- Склеродермия.
Оценивая данные КТ легких, врач-рентгенолог дифференцирует заболевания по специфической картине «матовых стекол»: их количеству, локализации, наличию других признаков, по которым возможно определить причину патологических изменений ткани легких. Например, для двусторонней вирусной пневмонии характерно наличие «матовых стекол», расположенных периферически в нижних и задних отделах легких. В более поздней стадии наблюдается консолидация очагов инфильтрации с утолщением перегородок альвеол.
Например, для двусторонней вирусной пневмонии характерно наличие «матовых стекол», расположенных периферически в нижних и задних отделах легких. В более поздней стадии наблюдается консолидация очагов инфильтрации с утолщением перегородок альвеол.
«Матовые стекла» при туберкулезе могут быть расположены рядом с бронхами или диссеминированы — в этом случае наблюдается множество маленьких светлых участков (инфильтратов), хаотично расположенных во всей полости легких. Также при туберкулезе на КТ легких можно обнаружить характерные фиброзные тяжи, ведущие к корню легкого — это перибронхиальное воспаление, признаки лимфостаза с увеличением лимфатических узлов. Единичные участки «матового стекла» малого размера без четкого паттерна какого-либо заболевания могут указывать на новообразование, развивающийся фиброз, аденокарциному (рак) легких.
Иногда «матовые стекла» указывают на сосудистые патологии, которые приводят к сдавливанию альвеолярного пространства. У пациентов с ожирением могут появится в гравитационно-зависимых (нижних) областях легких под воздействием лишнего веса.
Не принимая в расчет эти погрешности и говоря об истинном синдроме «матового стекла» на КТ легких, отметим, что это признак нефункциональных участков легких. В норме уплотнений и препятствий для дыхания быть не должно, а легочная ткань представлена на томограммах однородным темным цветом. Очень редко «матовые стекла» указывают на индивидуальные особенности организма пациента, например, на нетипичное расположение диафрагмы у новорожденных. Но это единичные случаи, поэтому давайте рассмотрим наиболее распространенные паттерны заболеваний, при которых на томографии встречаются «матовые стекла».
«Матовые стекла» на КТ при пневмонии
Чаще всего «матовое стекло» на КТ проявляется при воспалении легких, причем это может быть абсолютно любая пневмония: вирусная, бактериальная, с атипичным развитием симптомокомплекса, очень редкая интерстициальная и так далее.
Общим признаком острых пневмоний на КТ является наличие инфильтратов («матовых стекол») разной формы и протяженности. «Матовые стекла» расположены вокруг очагов или диффузно, как при туберкулезе. Однако в отличие от туберкулеза, их размер обычно больше, есть тенденция к консолидации инфильтратов и образованию рисунка по типу «булыжной мостовой». В отдельных случаях визуализируются просветы бронхов, содержащих газ. Это называется синдромом «воздушной бронхографии». В сочетании с эффектом «матового стекла», он также относится к явным признакам пневмонии.
Для пневмонии, вызванной коронавирусом COVID-19, характерно периферическое расположение очагов поражения под плеврой.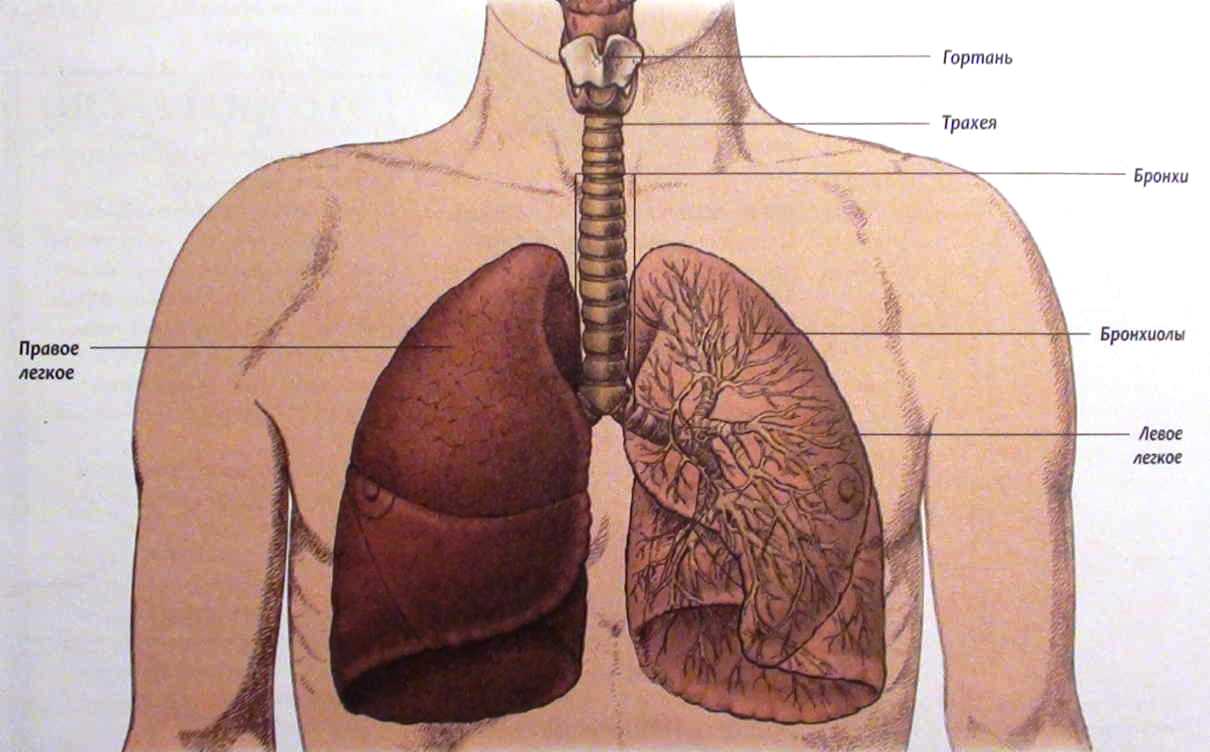 Наиболее уязвимы билатеральные нижние доли и задние отделы легких. Отмечается тенденция к консолидации «матовых стекол» и утолщению перегородок альвеол, иногда — признаки фиброза легких.
Наиболее уязвимы билатеральные нижние доли и задние отделы легких. Отмечается тенденция к консолидации «матовых стекол» и утолщению перегородок альвеол, иногда — признаки фиброза легких.
Тяжелым формам коронавирусной пневмонии сопутствует острый респираторный дистресс-синдром. ОРДС — это обширное двухстороннее воспаление, при котором наблюдается множество инфильтратов и отек легких. На томограммах фрагментарные участки «матового стекла» кортикальной формы присутствуют с двух сторон и имеют вид «лоскутного одеяла».
При пневмоцистной пневмонии, вызванной дрожжеподобным грибом Pneumocystis Jirovecii, наблюдается несколько иная картина. Участки уплотнения легких по типу «матового стекла» обычно расположены с двух сторон симметрично (но иногда диффузно и неравномерно). Уплотнения преобладают в прикорневых областях легких, а диффузные изменения — в верхних и нижних отделах. Для пневмоцистной пневмонии, как и для вирусной, ассоциированной с COVID-19, характерны эффект консолидации и симптом «лоскутного одеяла», но на томограммах легких видны и другие признаки: воздушные кисты, пневмоторакс.
Отдельную группу заболеваний представляют идиопатические интерстициальные пневмонии, причину которых не удается установить. Помимо «матового стекла» на сканах КТ легких можно обнаружить симптом «сотового легкого», бронхоэктазы, ретикулярные изменения. Идиопатические пневмонии требуют гистологического обследования.
На основании данных компьютерной томографии легких и анамнеза пациента врач-рентгенолог сможет определить поражение легких, характерное для пневмонии. В рамках дифференциальной диагностики учитывается плотность и форма «матовых стекол», их количество, в целом оценивается рисунок. Однако определить возбудителя пневмонии и тактику лечения можно после дополнительной лабораторной диагностики.
«Матовое стекло» на КТ при туберкулезе
Очаги инфильтрации по типу «матового стекла» встречаются и при туберкулезе. Его вызывает бактерия Mycobacterium tuberculosis. Считается, что все взрослые люди, достигшие возраста 30 лет, являются носителями микобактерии в «спящем» виде. Когда иммунитет подавлен, бактерии туберкулеза могут активизироваться, и человек заболеет.
Когда иммунитет подавлен, бактерии туберкулеза могут активизироваться, и человек заболеет.
При туберкулезе на КТ легких обычно видны множественные мелкие (милиарные) очаги, диссеминированные по легким. Возможна их концентрация в определенной доле. Часто присутствует инфильтрат в форме «дорожки», ведущей к корню легкого. Отмечается увеличение лимфатических узлов. Окончательно отличить туберкулез от пневмонии возможно по результатам ПЦР-диагностики — анализа крови на предмет возбудителя инфекционного воспаления легких.
«Матовое стекло» на КТ при отеке легких
Отёк легких — это осложнение массивного воспаления, сепсиса, токсического отравления. Отек часто возникает как осложнение хронических и острых заболеваний легких, следствие коронарной ишемии, сердечной недостаточности, патологических сбоев в работе других органов и их систем.
При кардиогенном отеке легких наряду с «матовыми стеклами» наблюдается утолщение междолевой плевры, сетчатая деформация легочного рисунка, а контуры корней легких расширенные и нечеткие.
К дополнительным признакам отека легких на КТ относится увеличение диаметра легочных сосудов, расширение камер сердца и жидкость в плевральной полости.
«Матовое стекло» при аденокарциноме (раке) легкого
По эффекту «матового стекла» на КТ легких определяют злокачественные новообразования — рак легких. Аденокарцинома — самый распространенный вид опухоли; существенным «спусковым механизмом» для ее образования является курение, наследственность, возраст (старше 40 лет).
Опухоль аденокарцинома формируется из клеток железистого эпителия. На томограмме представлена единичным обычно небольшим (от 2 мм) участком уплотнения по типу «матового стекла». В отдельных случаях у пациента наблюдается несколько «матовых стекол» диффузного или диффузно-мозаичного типа. Аденокарцинома представлена различными морфологическими подтипами и требует динамического наблюдения.
Не пытайтесь самостоятельно интерпретировать изображения. Выявить «матовые стекла» и дать им дифференцированную оценку может только профильный врач специалист, прошедший обучение и имеющий соответствующий сертификат.
Выявить «матовые стекла» и дать им дифференцированную оценку может только профильный врач специалист, прошедший обучение и имеющий соответствующий сертификат.
Текст подготовил
Котов Максим Анатольевич, главный врач центра КТ «Ами», кандидат медицинских наук, доцент. Стаж 21 год
- Iranmanesh A.M., Washington L. Pulmonary Sarcoidosis: A Pictorial Review / Semin Ultrasound CT MR, 2019.
- Felix J., Herth F., Kirby M., Sieren J., Herth J., Schirm J., Wood S., Schuhmann M. The Modern Art of Reading Computed Tomography Images of the Lungs: Quantitative CT / Respiration, 2018.
- Soussan M., Brillet P.-Y., Mekinian A., Khafagy A., Nicolas P., Vessieres A., Brauner M. Patterns of pulmonary tuberculosis on CT / Eur J Radiol, 2012.
- Bushong S. Computed Tomography / McGraw Hill Professional – 2000. – 162 p.
- Boyd D.P, Computed tomography: physics and instrumentation / Acad Radiol – 1995.

- Котов М.А. Опыт применения компьютерной томографии в диагностике заболеваний органов дыхания у детей / Материалы X Невского радиологического Форума (НРФ-2018). – СПб., 2018, Лучевая диагностика и терапия. 2018. № 1 (9). — С. 149.
- Карнаушкина М.А., Аверьянов А.В., Лесняк В.Н. Синдром «матового стекла» при оценке КТ-изображений органов грудной клетки в практике клинициста: патогенез, значение, дифференциальный диагноз / Архивъ внутренней медицины – М., 2018. — С. 165-175.
- Прокоп М., Галански М. Спиральная и многослойная компьютерная томография / Т.1,2 под ред. А.В.Зубарева, Ш.Ш.Шотемора — М., 2011 — 712 с.
Снимки рака легких: Рентгеновские снимки и многое другое
Существуют различные типы рака легких, в зависимости от того, где они развиваются и какие у них особенности. Определение типа может помочь врачу посоветовать человеку подходящие варианты лечения и перспективы.
Рак легкого может начаться в различных частях легкого, например, в верхней, средней или внешней оболочках. Они также могут различаться по гистологии или структуре.
Они также могут различаться по гистологии или структуре.
Ряд инструментов может помочь в диагностике рака легких, включая сканирование легких. Сканирование может показать местоположение и тяжесть рака и даже указать его тип.
В этой статье мы обсудим, как может выглядеть рак легких на рентгенограмме или иначе. Мы также рассмотрим различные типы и различия между ними.
Двумя основными типами являются мелкоклеточный рак легкого (МРЛ) и немелкоклеточный рак легкого (НМРЛ). SCLC растет быстрее и труднее поддается лечению. Внутри НМРЛ также существуют подтипы, такие как аденокарцинома и плоскоклеточный рак.
Характеристики рака легких будут зависеть от типа, который, в свою очередь, повлияет на путь развития рака и перспективы.
Ниже приведены некоторые характеристики различных типов рака легких.
SCLC
SCLC составляет около 15% случаев рака, которые развиваются в дыхательных путях. Курение является основным фактором риска. Однако воздействие асбеста, радиации и загрязнения воздуха также увеличивает риск.
Существует два подтипа: мелкоклеточная карцинома, или овсяноклеточный рак, и комбинированная мелкоклеточная карцинома.
У человека с ограниченной стадией SCLC будет рак в области, где он начался, или рядом с ней. Если у человека расширенная стадия SCLC, он распространится на другие части тела, и его будет труднее лечить.
SCLC имеет тенденцию к более быстрому росту, чем другие типы рака легких, и его трудно лечить. Тем не менее, около 27% людей, которым поставили диагноз на ранней стадии, проживут еще 5 и более лет.
На рентгенограмме грудной клетки эти опухоли могут выглядеть как белые массы, расположенные ближе к центру легких.
НМРЛ
Существует несколько типов НМРЛ. Тип будет зависеть от того, где он начинается в легких.
Немелкоклеточный рак легкого относится к любому раку, поражающему клетки легкого, который не является мелкоклеточным раком легкого. Примеры включают:
- аденокарцинома
- плоскоклеточный рак
- крупноклеточный рак
Курение, воздействие асбеста и других токсинов, а также наличие ВИЧ – все это возможные факторы риска.
NSCLC растет медленнее, чем SCLC. Человек, получивший диагноз на самой ранней стадии, будет иметь 63-процентный шанс прожить как минимум еще 5 лет.
Аденокарцинома
Около 40% случаев рака легкого приходится на аденокарциному, которая является разновидностью НМРЛ. Обычно он начинается в наружных отделах легких и медленно растет. Существует несколько типов аденокарциномы.
Аденокарцинома начинается в наружной части легких и развивается в виде круглых узелков в легких. Узелки сначала появляются в клетках, вырабатывающих слизь.
Курение является основным фактором риска аденокарциномы. Однако этот тип рака легких чаще всего развивается у некурящих.
Плоскоклеточный рак
Около 25% всех случаев рака легких приходится на плоскоклеточный рак. Этот тип начинается в клетках, выстилающих дыхательные пути в легких.
Опухоли обычно появляются вблизи одного из главных дыхательных путей легкого. По мере роста опухоли они могут проникать в стенку грудной клетки.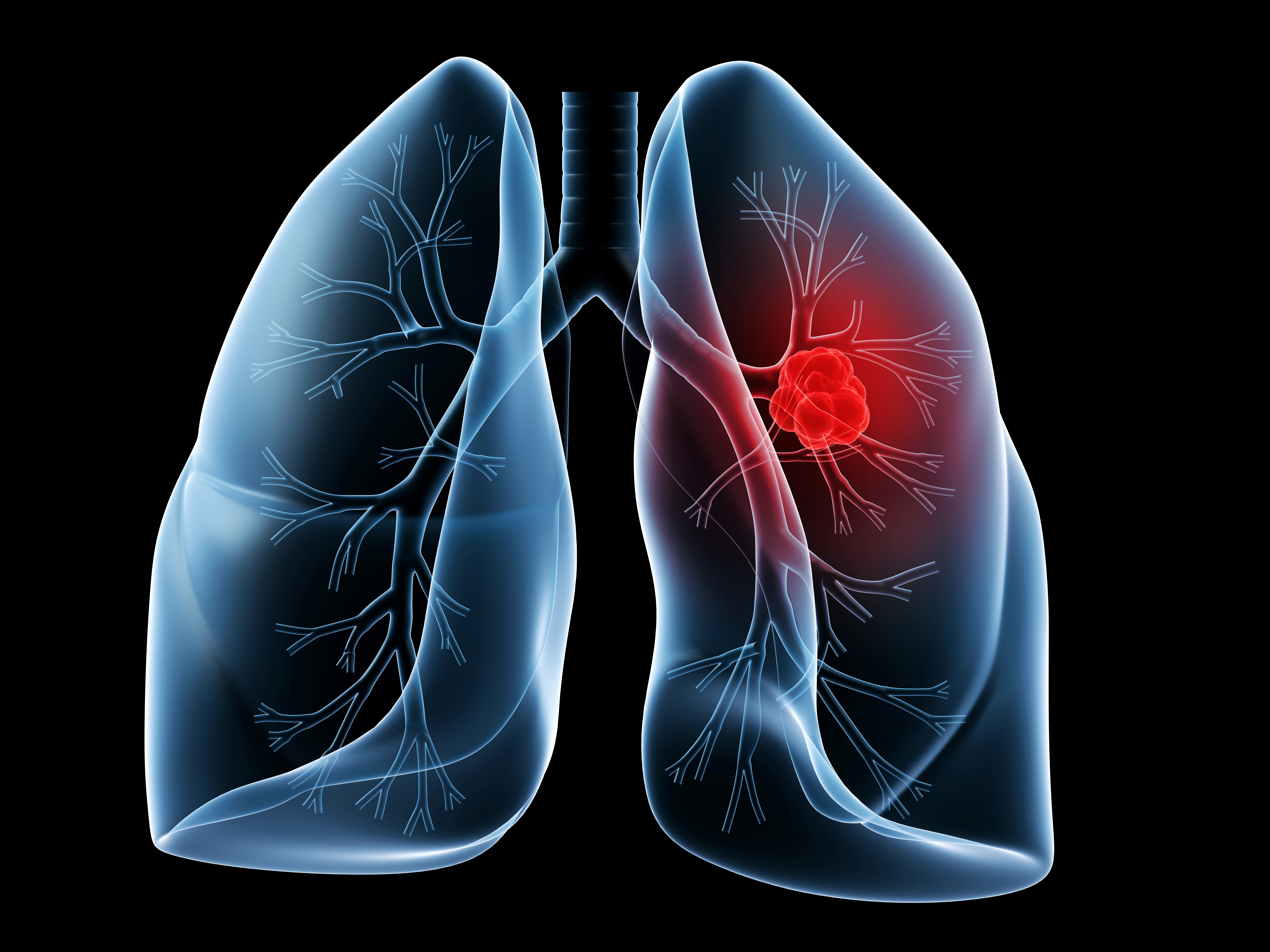
Крупноклеточный (недифференцированный) рак
На этот тип рака приходится около 10% всех случаев рака легких.
Он может появиться в любом месте легких и быстро растет. Это затрудняет лечение.
Мезотелиома
Слой клеток, называемый мезотелием, окружает легкие, сердце, брюшную полость и другие органы. Плевра, разновидность мезотелия, окружает легкие.
Мезотелиома плевры, или просто мезотелиома, представляет собой рак, который сначала развивается в этом слое ткани.
По данным Американского онкологического общества (ACS), рентген грудной клетки может выявить:
- утолщение плевры
- отложения кальция на плевре
- жидкость между легкими и грудной стенкой
- другие изменения в легкие, которые могут свидетельствовать о мезотелиоме
Опухоль Панкоста
Опухоли Панкоста являются редким типом рака легких. Они развиваются в верхней части легкого и составляют 3–5% случаев рака легких.
Опухоли Панкоста вызывают комплекс симптомов из-за близлежащих структур, которые они могут поражать. Симптомы включают онемение пальцев или рук, чрезмерное потоотделение и синдром Горнера.
Метастатический рак
Когда рак распространяется за пределы места, где он впервые образовался, это метастазы.
Рак может распространяться из исходного места в другие части тела через кровь. Опухоль также может распространяться, прорастая в близлежащие ткани.
Метастатический рак легкого — это рак, который распространился на другую часть тела, например, в печень. В данном случае это все же рак легких.
Если у человека рак молочной железы, который достигает легкого, это не будет раком легкого. Это будет метастатический рак молочной железы.
Врач будет использовать рентген грудной клетки при диагностике любого типа рака, потому что другие виды рака часто распространяются на легкие.
Врач может порекомендовать пройти обследование на рак легких, если у человека постоянный кашель, боль в груди или хрипота. Они также могут обнаружить признаки рака легких во время регулярного осмотра.
Они также могут обнаружить признаки рака легких во время регулярного осмотра.
Врач начнет с того, что расспросит человека о:
- симптомы
- их семейная и личная история болезни
- факторы образа жизни, такие как курение
Они также проведут медицинский осмотр.
Если они считают, что у человека может быть рак легких, они порекомендуют некоторые анализы.
Рентген грудной клетки
Рентген грудной клетки обычно является первым тестом, но для подтверждения наличия рака потребуются дополнительные тесты.
Если рентген показывает рост, это не обязательно рак.
По данным Американского торакального общества, до 50% взрослых, которым сделали рентген грудной клетки или компьютерную томографию легких, имеют по крайней мере один новообразование. Однако менее 5% этих новообразований являются злокачественными.
Компьютерная томография и другие виды сканирования
При компьютерной томографии используются несколько рентгеновских изображений для создания подробного изображения легких. Он более надежен, чем рентген, для выявления опухолей легких.
Он более надежен, чем рентген, для выявления опухолей легких.
Он также может показать размер, форму и положение опухоли, а также определить, поражает ли рак лимфатические узлы и другие части тела.
ПЭТ также может предоставить более подробную информацию. Врач может порекомендовать ПЭТ-сканирование вместе с компьютерной томографией для получения более подробного впечатления.
Биопсия и лабораторные анализы
Биопсия легкого — единственный способ подтвердить наличие рака легкого.
Это включает взятие небольшого образца легочной ткани для исследования под микроскопом. Результаты могут показать, есть ли рак, и если да, то какой тип.
Врач может также предложить анализ мокроты. В этом случае они возьмут образец мокроты, чтобы отправить его в лабораторию для анализа.
Рак легкого легче всего лечить на ранних стадиях, но у людей часто симптомы на ранних стадиях отсутствуют.
Однако, если симптомы появляются, они включают в себя:
- боль в груди
- Кашель.
 лицо или шея
лицо или шея
По мере роста и распространения рака легких могут появляться и другие симптомы.
Узнайте больше о признаках и симптомах рака легких здесь.
Варианты лечения зависят от типа рака легкого, стадии и факторов, специфичных для каждого человека.
Врач может порекомендовать одно или несколько из следующего:
- химиотерапия
- хирургия
- таргетная терапия
- иммунотерапия
- лучевая терапия план.
Изменения образа жизни, такие как здоровое питание, физические упражнения и отказ от курения, также могут помочь продлить жизнь человека и уменьшить тяжесть симптомов.
Перспективы развития рака легких зависят от:
- стадии рака на момент постановки диагноза
- типа рака
- возраста и общего состояния здоровья человека
диагноз, изучая прошлые цифры.
According to the ACS, the chances of surviving 5 years or more with SCLC and NSCLC are as follows:
Stage NSCLC SCLC localized (still in исходное местонахождение) 63% 27% региональный (распространился на близлежащие районы) 35% 16% метастатический0211 7 % 3 % в целом 25 % 7 % Врач может посоветовать эффективные способы сделать это.

В Интернете также можно приобрести продукты, которые могут помочь людям бросить курить.
Прочитайте эту статью на испанском языке.
Появляется более полная молекулярная картина плоскоклеточного рака легкого
Рак легких остается ведущей причиной смерти от рака в Соединенных Штатах и во всем мире. Пациенты с подтипом, называемым аденокарциномой легкого (LUAD), получили пользу от разработки новых таргетных лекарств, но поиск эффективных новых методов лечения другого подтипа, называемого плоскоклеточным раком легкого (LSCC), в значительной степени не увенчался успехом.
Чтобы узнать больше о биологической основе LSCC, группа исследователей из Института Броуда Массачусетского технологического института и Гарварда, а также Консорциума клинического протеомного анализа опухолей (CPTAC) Национального института рака, включая сотрудников из Медицинского колледжа Бейлора, разработала самая большая и наиболее полная молекулярная карта LSCC на сегодняшний день.
 Их усилия, описанные в Cell объединяет протеомные, транскриптомные и геномные данные в подробное «протеогеномное» представление о LSCC. Анализ этих данных выявил потенциальные новые мишени для лекарств, пути иммунной регуляции, которые могут помочь раку избежать иммунотерапии, и даже новый молекулярный подтип LSCC. Данные исследования доступны на портале CPTAC.
Их усилия, описанные в Cell объединяет протеомные, транскриптомные и геномные данные в подробное «протеогеномное» представление о LSCC. Анализ этих данных выявил потенциальные новые мишени для лекарств, пути иммунной регуляции, которые могут помочь раку избежать иммунотерапии, и даже новый молекулярный подтип LSCC. Данные исследования доступны на портале CPTAC.«Пациенты с плоскоклеточным раком легкого имеют очень ограниченные терапевтические возможности, и даже скромный успех в понимании этого заболевания может изменить жизнь людей», — сказал Шанха Сатпати, руководитель группы протеомики Института Броуда и один из первых и соавтор 9Исследование 0267 Cell с соавторами Карстеном Кругом и Пьером Жан-Бельтраном из Broad и Сарой Сэвидж из Baylor. «Мы надеемся, что исследовательское сообщество, от фундаментальных ученых до практикующих онкологов, будет использовать этот новый ресурс для проверки гипотез, стимулирования дальнейших исследований и открытия новых основанных на данных возможностей для дизайна клинических испытаний, которые в долгосрочной перспективе могут принести пользу пациентам.
 .»
.»Целевые возможности
В своем исследовании команда проанализировала ДНК, РНК, белки и посттрансляционные модификации белков (PTM, то есть фосфорилирование, ацетилирование и убиквитинирование) 108 опухолей до лечения и сравнила их с нормальной тканью. Среди возможностей, которые они увидели для разработки новых методов лечения LSCC, исследователи определили ген 9.0267 NSD3 в качестве возможной мишени для опухолей, содержащих дополнительные копии FGFR1 , другого гена, который часто дублируется или амплифицируется при LSCC. Предыдущие попытки безуспешно пытались напрямую нацелиться на FGFR1 . Протеогеномные данные группы показывают, что NSD3 может быть критическим фактором роста и выживания в этих опухолях, что делает его потенциальной терапевтической мишенью.
Они также отметили подгруппу пациентов, у которых в опухолях была обнаружена низкая экспрессия p63, но высокая экспрессия сурвивина, белка, который регулирует пролиферацию и гибель клеток и является объектом клинических испытаний при других типах опухолей.

Кроме того, данные группы показали, что опухоли, вызванные гиперэкспрессией фактора транскрипции SOX2, могут быть уязвимы для лечения, направленного против модификаторов хроматина, таких как LSD1 и EZh3. Сам SOX2 обычно считается «не поддающейся лечению» мишенью; наблюдения группы указывают на возможность разработки терапевтического обходного пути.
«Данные протеомики и PTM помогают нам увидеть функциональные эффекты генома», — объяснил Майкл Джиллетт, старший руководитель группы протеомики в Broad, лечащий врач отделения легочной и интенсивной терапии в Массачусетской больнице общего профиля и соавтор. старший автор исследования со Стивеном Карром и доктором Мани из Broad и Бинг Чжан из Baylor. «Понимание того, на какие уровни белка влияют изменения числа копий, и как мутации влияют на экспрессию белка и активность пути, позволяет глубже понять биологию рака».
«Часто эти идеи намекают на неизведанные терапевтические возможности или на определенные группы населения, которым может быть полезно конкретное лечение», — добавил он.
 «Это особенно важно при таком заболевании, как LSCC, многие клинические испытания которого потерпели неудачу».
«Это особенно важно при таком заболевании, как LSCC, многие клинические испытания которого потерпели неудачу».Иммунные исследования
Несмотря на то, что иммунотерапия представляет собой самый большой прогресс в терапии LSCC за последние десятилетия, результаты лечения пациентов отстают от результатов, наблюдаемых при LUAD; только у меньшинства пациентов с LSCC наблюдается долгосрочный ответ. Основываясь на своих протеогеномных данных, команда представила подробную картину иммунного ландшафта LSCC, выделив несколько путей иммунной регуляции, которые могут служить целевыми точками. В частности, их анализ выявил подмножество опухолей, которые демонстрируют маркеры, связанные с реакцией на ингибиторы иммунных контрольных точек (такие как блокаторы PD-1/PD-L1) и с уклонением от иммунного ответа, что дает некоторые подсказки относительно того, почему результаты иммунотерапии настолько неравномерны в разных группах. пациентов с ЛСКК.
«Более глубокое понимание иммунного ландшафта опухолей LSCC может в конечном итоге привести к более эффективной иммунотерапии и маркерам для стратификации пациентов», — сказал Чжан, профессор Центра груди Лестера и Сью Смит и отдела молекулярной и генетики человека в Бэйлоре.
 .
.Обнаружена метаболическая дисрегуляция и перекрестные помехи
Убиквитинирование — это процесс, при котором клетка помечает белки другим небольшим белком, называемым убиквитином (или его биохимическими родственниками), чтобы нацелить их на уничтожение. Хотя этот процесс важен для нормального функционирования, при нарушении его регуляции он может способствовать заболеванию или привести к нему. Ранее команда Broad разработала UbiFast, технологию, позволяющую проводить глубокомасштабный и высокопроизводительный анализ убиквитилирования в образцах тканей пациентов. Применительно к LSCC UbiFast выявил сложную регуляцию метаболических путей, таких как гликолиз и окислительный стресс, обусловленный молекулярными перекрестными помехами, основанными на убиквитилировании (или убиквитин-подобных модификациях) и двух других формах модификации белка, фосфорилировании (которое изменяет ферментативную или каталитическую активность белка). и ацетилирование (которое может повлиять на структуру, активность, локализацию и стабильность белка).

Появление нового подтипа
Предыдущие исследования выявили четыре молекулярных подтипа LSCC с использованием геномики, соответствующих различным типам клеток и процессам. С их протеомной точки зрения исследовательская группа не только получила более глубокое понимание иммунных, метаболических и пролиферативных сигналов, связанных с этими подтипами, но также обнаружила новый подтип эпителиально-мезенхимального перехода. Они отметили, что клетки этого нового типа могут иметь больший потенциал для метастазирования, но также имеют активные молекулярные пути, управляемые киназой, которые могут быть нацелены терапевтически.
«Это примечательно, потому что в опухолях LSCC обычно отсутствуют типы изменений киназы, присутствующие в LUAD, которые послужили основой для разработки широкого спектра терапевтических ингибиторов», — сказала Ана Роблес, программный директор отдела клинических протеомных исследований рака NCI.
Участники исследования выполняли свою работу под эгидой CPTAC, спонсируемой NCI междисциплинарной/межведомственной организации, направленной на ускорение понимания молекулярных основ рака путем применения крупномасштабного протеогеномного анализа.


 лицо или шея
лицо или шея
 Их усилия, описанные в Cell объединяет протеомные, транскриптомные и геномные данные в подробное «протеогеномное» представление о LSCC. Анализ этих данных выявил потенциальные новые мишени для лекарств, пути иммунной регуляции, которые могут помочь раку избежать иммунотерапии, и даже новый молекулярный подтип LSCC. Данные исследования доступны на портале CPTAC.
Их усилия, описанные в Cell объединяет протеомные, транскриптомные и геномные данные в подробное «протеогеномное» представление о LSCC. Анализ этих данных выявил потенциальные новые мишени для лекарств, пути иммунной регуляции, которые могут помочь раку избежать иммунотерапии, и даже новый молекулярный подтип LSCC. Данные исследования доступны на портале CPTAC. .»
.»
 «Это особенно важно при таком заболевании, как LSCC, многие клинические испытания которого потерпели неудачу».
«Это особенно важно при таком заболевании, как LSCC, многие клинические испытания которого потерпели неудачу».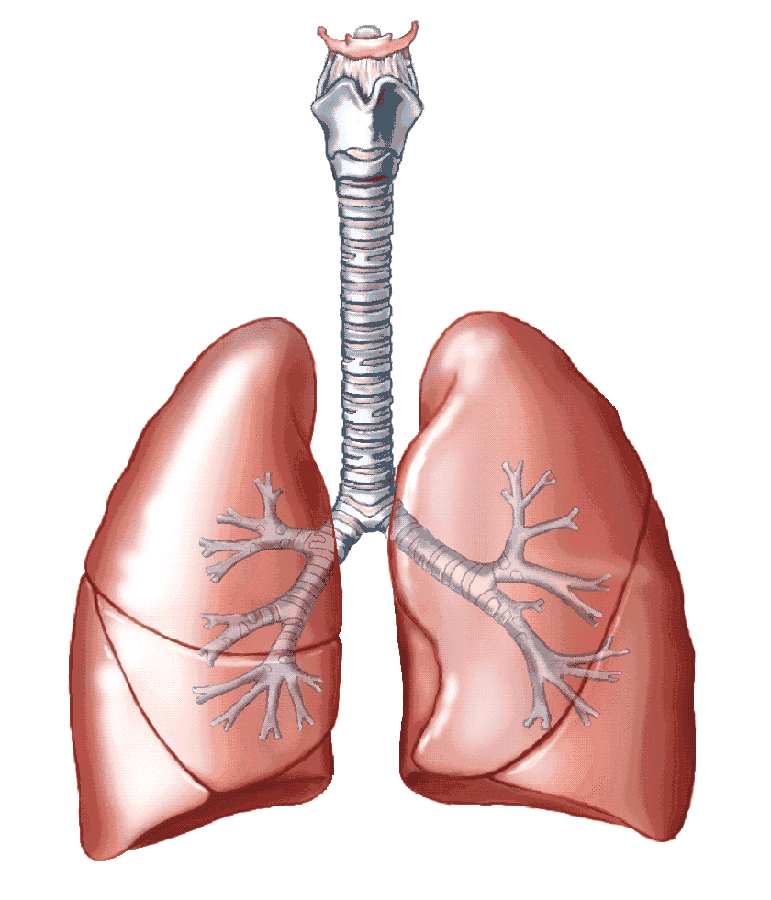 .
.
